Biochemie
Bisher unbekannte Proteindomäne sorgt für Kollagentransport
Die Entdeckung der MOTH-Domäne erlaubt Einblicke in die Evolution. Denn sowohl Insekten als auch Wirbeltiere benötigen Kollagen in ihrem Bindegewebe.
Kollagen ist das Protein, das unseren Körper zusammenhält. Produziert wird es innerhalb von Zellen, dann muss es an seinen Wirkungsort im Bindegewebe transportiert werden. Für die Erkennung des Kollagens ist eine Proteindomäne zuständig, die bislang als Unterform einer anderen verkannt wurde. Dr. Oliver Arnolds und Prof. Dr. Raphael Stoll aus der Fakultät für Chemie und Biochemie der Ruhr-Universität Bochum haben diese Domäne erstmals charakterisiert und getauft: Über die sogenannte MOTH-Domäne der TANGO1-Proteinfamilie berichten sie in der Zeitschrift Nature Communications vom 20. April 2023.
Wie Kollagen an seinen Wirkungsort gelangt
Nahezu alle Organismen mit mehr als einer Zelle brauchen Kollagen, das ihren Körper zusammenhält. Bei manchen Säugetieren macht es bis zu 30 Prozent des Körpergewichts aus. Das Kollagen – ein riesiges Protein – wird im sogenannten Endoplasmatischen Retikulum hergestellt, einem Organell innerhalb von Zellen. Dann muss es aus dem Organell und aus der Zelle herausgeschleust werden, denn es wird im Raum zwischen den Zellen im Bindegewebe gebraucht.
Für die Erkennung und den Transport des Kollagens ist eine Proteinfamilie namens TANGO1 zuständig. Die dazugehörigen Proteine sind mit mehr als 1.000 Aminosäuren sehr groß. TANGO1-Proteine durchspannen mitunter verschiedene Zellorganellen und die Zellflüssigkeit. Erkennt das TANGO1-Protein ein fertiges Kollagen, unterstützt es die Bildung einer tunnelartigen Lipidschleuse, die das Kollagen von seinem Herstellungs- an seinen Wirkungsort befördert.
Eine ganz eigene Struktur
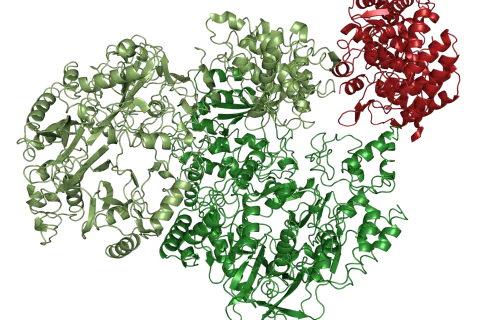
Für diese Mechanismen verfügt TANGO1 über eine bestimmte Domäne, also einen funktionellen Bereich mit einer definierten 3D-Struktur. „Bisher hat man angenommen, dass diese Domäne ähnlich der sogenannten SH3-Struktur ist, und sie als eine Unterstruktur angesehen“, erklärt Raphael Stoll. In der aktuellen Arbeit konnten er und Oliver Arnolds jedoch mittels NMR-Spektroskopie nachweisen, dass es zwischen der Kollagenerkennungsdomäne von TANGO1 und der SH3-Domäne strukturelle Unterschiede gibt, die biochemisch so bedeutend sind, dass sie es rechtfertigen, bei TANGO1 von einer eigenen Struktur zu sprechen. Sie tauften die Kollagen-erkennende Domäne MOTH (auf Deutsch: Motte). „Der Name ist eine Abkürzung für die insgesamt vier Proteine, welche genau diese Struktur aufweisen: MIA, Otoraplin, TALI/TANGO1-Homologie“, erklärt Raphael Stoll.
Die Entdeckung der MOTH-Domäne erlaubt Einblicke in die Evolution, denn sowohl Wirbeltiere als auch Wirbellose wie Insekten brauchen Kollagen. „Die MOTH-Domäne ist evolutionär sehr alt, mehrere hundert Millionen Jahre“, so Raphael Stoll. Mit der Trennung der Wirbellosen von den Wirbeltieren hat sich die Domäne während der Evolution allerdings verändert. „Wir nehmen an, dass dies mit der Entwicklung mehrerer verschiedener Kollagene einhergeht. Während Insekten nur ein Kollagen haben, findet man beim Menschen 28 verschiedene Variationen davon. Diese Ergebnisse tragen zu einem verbesserten Verständnis des Kollagen-Exportprozesses bei und könnten sich bei zukünftigen Medikamentenentwicklungen für Fibrosen als nützlich erweisen“, so Stoll.