Biologie
Altes Gelbes Enzym hilft Algen gegen Lichtstress
Seit fast 100 Jahren sind Alte Gelbe Enzyme bekannt, doch ihre Funktion für Organismen liegt größtenteils im Dunkeln. Ein Bochumer Forschungsteam veröffentlicht erste Erkenntnisse zu Mikroalgen.
Alte Gelbe Enzyme, kurz OYEs, vom englischen Old Yellow Enzymes, wurden in den 1930er-Jahren entdeckt und seitdem stark erforscht. Denn diese Biokatalysatoren – gelb gefärbt durch ein Hilfsmolekül – können Reaktionen durchführen, welche für die chemische Industrie sehr wertvoll sind, etwa Medikamentenvorstufen oder Duftststoffe herstellen. Obwohl OYEs in vielen Organismen vorkommen, ist ihre natürliche Rolle für diese Lebewesen bisher kaum bekannt – möglicherweise, weil der wissenschaftliche Fokus auf der biotechnologischen Anwendung lag. Forschende um Privatdozentin Dr. Anja Hemschemeier und Prof. Dr. Thomas Happe von der Ruhr-Universität Bochum zeigen nun, dass ein OYE der einzelligen Grünalge Chlamydomonas reinhardtii wichtig für den pflanzlichen Einzeller ist, um sich vor Lichtstress zu schützen. Die Forschenden haben ihre Ergebnisse in der Zeitschrift „Plant Direct“ vom 15. Januar 2023 veröffentlicht.
OYEs in Mikroalgen nutzen Energie aus der Fotosynthese
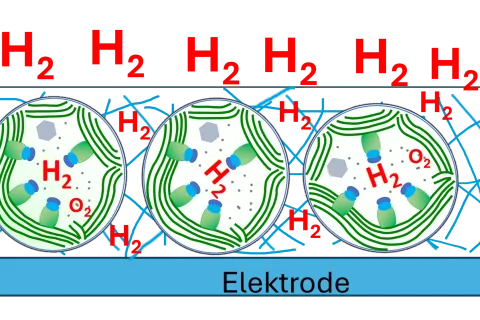
„Unsere Arbeitsgruppe gehört zu den ersten, die OYEs in Algen untersuchen“, erzählt Dr. Stefanie Böhmer, Erstautorin der Studie. „Zunächst wollten wir untersuchen, ob diese Biokatalysatoren auch für industrielle Prozesse geeignet sind. Besonders interessant war für uns, ob Mikroalgen die Energie der Fotosynthese nutzen können, um die entsprechenden chemischen Reaktionen anzutreiben. Dies könnte helfen, umweltfreundlichere Produktionen zu etablieren.“ Die Forschenden konnten dies tatsächlich nachweisen: Ein zu lebenden Algenzellen zugefügtes chemisches Molekül wurde nur im Licht mit hohen Raten umgesetzt. „Dieses Ergebnis deutete aber auch darauf hin, dass die dafür verantwortlichen sogenannten En-Reduktasen in den Algen mit der Fotosynthese zusammenhängen“, so Böhmer. Daher untersuchten die Wissenschaftlerinnen und Wissenschaftler der Arbeitsgruppe Photobiotechnologie, wie sich ein Algenstamm, in welchem ein OYE-Biokatalysator defekt ist, an Starklicht anpasst.
Überschüssige Lichtenergie muss abgeleitet werden
Tatsächlich konnte das Bochumer Forschungsteam in Kooperation mit Forschenden der Universität Leipig zeigen, dass dieser Algenstamm kaum in der Lage ist, überschüssige Lichtenergie abzuleiten. „Fotosynthetische Lebewesen wie Algen und Pflanzen müssen stets das Gleichgewicht zwischen aufgenommener Lichtenergie und deren Umsetzung in chemische Energie aufrechterhalten“, erklärt Anja Hemschemeier, unter deren Federführung die Studie durchgeführt wurde. „Bei zu starkem Licht kommt es sonst zu oxidativen Zellschäden. Daher besitzen diese Lebewesen ausgeprägte Schutzmechanismen, um überschüssige Lichtenergie abzuleiten, zum Beispiel als Wärme.“
In dem Mikroalgenstamm, dem ein OYE fehlt, konnten die Forschenden diese Schutzmechanismen kaum noch nachweisen, und der Stamm wies dementsprechend oxidative Schäden auf. „Wir vermuten, dass ein bestimmtes Molekül, das von diesem Biokatalysator in den Algenzellen normalerweise umgesetzt wird, wichtig für das fotosynthetische Gleichgewicht ist“, so Hemschemeier.
Dem will das Forschungsteam nun weiter auf den Grund gehen. „Fotosynthetische Organismen sind die Grundlage für unser Leben. Es ist sehr wichtig zu verstehen, wie sie sich an Stressbedingungen anpassen, und wir glauben, hier ein weiteres Puzzlestück gefunden zu haben“, schließt Hemschemeier.