Lara Marson, Doktorandin am Lehrstuhl für Angewandte Mikrobiologie, untersucht, welche natürlichen Derivate von Calcimycin durch Wildtyp- und Mutantenstämme unter unterschiedlichen Kultivierungsbedingungen produziert werden.
Mikrobiologie
Piraterie unter Mikroben
Bakterien brauchen Eisen für ihr Wachstum. Kommen sie aus eigener Kraft nicht gut genug heran, beklauen sie ihre Nachbarn.
Im Boden gönnt man einander nichts. Eine Milliarde Bakterien leben in einem Gramm Erde, dazu noch Pilze. Und es tobt ein steter Konkurrenzkampf zwischen den Mikroben. Es wird mit harten Bandagen gekämpft, vor allem dann, wenn Nährstoffe knapp oder schwer zugänglich sind. Die Methoden, mit denen die Kleinstlebewesen einander angehen, schaut sich Prof. Dr. Julia Bandow mit ihrem Team ganz genau an. Fernziel: Neue Substanzen entdecken, die sich als Antibiotika für den klinischen Einsatz eignen. „Auch Penicillin ist eine Substanz, die ein Pilz ausschüttet, um konkurrierende Bakterien zu töten und dabei deren Inhaltsstoffe freizusetzen, die dann verdaut werden können“, gibt sie ein Beispiel.
Eisen als limitierender Faktor
Aktuell konzentrieren sich die Forschenden darauf, wie Bakterien an die für ihr Wachstum nötigen Mikronährstoffe kommen. Dazu gehören unter anderem Mangan und Eisen, die zwar nur in geringer Menge gebraucht werden, ohne die aber kein Wachstum möglich ist. „Eisen ist ein Element, das es zwar überall im Überfluss gibt“, sagt Julia Bandow. „Aber es liegt überwiegend in schlecht wasserlöslicher Form vor und ist für die Organismen deswegen nur schlecht zugänglich.“ Eisen ist einer der limitierenden Faktoren für das Bakterienwachstum. „Wäre es einfach zu haben, würden nährstoffreiche Standorte binnen kurzem von einer zentimeterdicken Bakterienschicht überwuchert sein“, so die Forscherin.
Entsprechend haben Bakterien verschiedene Methoden entwickelt, trotzdem an Eisen heranzukommen. Diese Methoden sind unterschiedlich gut. Ist viel Eisen im Boden vorhanden, genügt ein Aufnahmesystem. Ist Eisen vorhanden, liegt aber beispielsweise an organisches Material gebunden vor, werden eisenbindende Moleküle, sogenannte Siderophore, gebildet, die strukturell einfach sind, wie Citrat. Bei noch weniger Eisenangebot kommen komplexe Siderophore wie Hydroxamate und Catecholate infrage, um an Eisenatome zu kommen.
Die Königsdisziplin in der Verfügbarmachung von Eisen sind in der Tat Catecholate. „Wir haben mit dem Bodenbakterium Bacillus subtilis einen wahren Spezialisten darin“, sagt Julia Bandow. „Es ist in der Lage, Catecholat-Siderophore zu bilden, die alle anderen Methoden zur Eisengewinnung übertreffen.“ Das lässt sich das Bakterium allerdings auch einiges kosten. Schon die Bildung dieser Moleküle ist mit einigem Aufwand verbunden, weil die Synthese eine Reihe von Proteinen erfordert. Werden die Siderophore ausgeschüttet, bilden sie einen wasserlöslichen Komplex mit Eisen, der dann unter Energieaufwand durch die Zellhülle importiert werden muss. Ist der Komplex im Inneren des Bakteriums, muss er aufwändig zerlegt werden, um das Eisen freizusetzen. „Bacillus subtilis setzt diese Methode der Eisenbeschaffung deswegen auch nur bei Eisenmangel ein“, erklärt Julia Bandow, „sonst nutzt es einfachere Substanzen.“ Allerdings sammelt das Bakterium auch Eisen und hortet es in seinem Inneren, damit immer ausreichend für das Wachstum zur Verfügung steht.
Die Kultivierung von Streptomyces chartreusis auf Festmedium dient der Erzeugung von Bakteriensporen.
Ganz anders haushaltet einer seiner Konkurrenten, Streptomyces chartreusis. Auch dieses Bodenbakterium ist in der Lage, Eisen aus der Umgebung in sein Inneres zu bringen. Es nutzt dafür Hydroxamat-Siderophore, die ausreichen, solange Eisen mindestens mittelmäßig gut verfügbar ist. Bei Eisenmangel, wenn nur noch Catecholate helfen, setzt Streptomyces auf eine andere Taktik: Es klaut bei seinen Nachbarn. „Dazu verfügt es über Aufnahmesysteme für fremde Siderophore“, erklärt Julia Bandow. „Diese Strategie ist unter Bakterien recht verbreitet. Man findet sie auch in Bakterien, die den Menschen besiedeln.“
Werkzeuge für den Eisenklau
Streptomyces chartreusis verfügt über ein zweites Werkzeug, das sich zum Klau von Eisenatomen eignet. Die Forschenden untersuchen Ionophore als Schlüsselsubstanzen, allen voran Calcimycin.
Diese Moleküle, die Streptomyces herstellen kann, sind im Urzustand wasserlöslich, sodass sie die Lipidmembran des Bakteriums schlecht passieren können. Das klappt erst gut, wenn sie eine Verbindung mit einem Metallatom eingehen. In diesem Moment kehrt sich die wasserlösliche Seite des Moleküls zum Metall nach innen, und es kann in dieser Form ohne Energieaufwand die lipophile Schicht der Zellmembran passieren.

Dr. David Podlesainski leitet das Mass Spectrometry Core for Life Sciences (MCLS) an der Fakultät für Biologie und Biotechnologie. Er führt Element-Analysen durch, die Auskunft über die Metallzusammensetzung biologischer Proben geben.
Die Forschenden isolierten Calcimycin und beobachteten, wie sich die Substanz auf Bacillus subtilis auswirkt. Dazu nutzten sie ein von der Ruhr-Universität beschafftes ICP-Massenspektrometer – ICP steht für inductively coupled plasma –, das feinste Spuren von Metallen messen kann. „Allein den Workflow zu etablieren, hat uns viel Zeit gekostet“, erzählt Julia Bandow. „Denn die kleinste Verunreinigung kann das Messergebnis verfälschen. Daher darf man bei der Probenvorbereitung weder Schmuck tragen noch Handcreme verwenden und muss Handschuhe tragen.“
Es zeigte sich: Setzt man Bacillus dem Ionophor aus, verliert es an Eisen und Mangan. „Im Austausch reichert sich Calcium, welches in der Umgebung der Zelle in hohen Konzentrationen verfügbar ist, in der Zelle an“, unterstreicht Julia Bandow. „Es handelt sich um Ionophor-vermittelte Diffusion entlang von Gradienten. Man stellt sich Diffusionsprozesse immer langsam vor – aber auf der Größenskala von Mikroben sind sie sehr schnell.“ Der Verlust der Mikronährstoffe regt das Bacillus zur Herstellung von mehr Siderophoren an, mit deren Hilfe es seine Eisenvorräte versucht wieder aufzustocken.
Um mehr über die zugrunde liegenden Prozesse herauszufinden, nutzt das Forschungsteam verändertes Calcimycin. Es zeigte sich: Hängt man ein Bromatom an das Ionophor, ändert sich seine Funktion. Dann kann es kein Eisen mehr transportieren, stattdessen aber Kupfer.
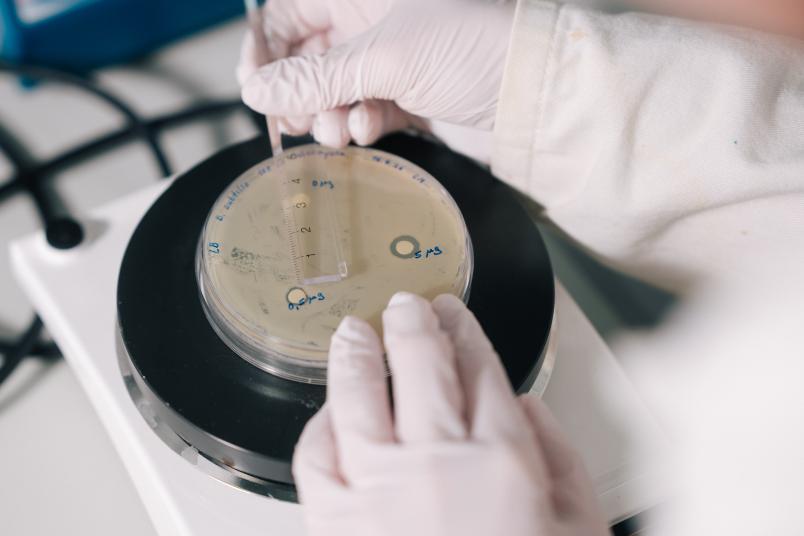
Aufgereinigte Ionophore hemmen das Wachstum des Bodenbakteriums Bacillus subtilis auf Nähr-Agar. Die Größe der Hemmhöfe im Bakterienrasen um die Calcimycin-getränkten Filterplättchen steigt mit steigender Ionophor-Konzentration.
Das Team reinigte die vom Bakterium produzierten Ionophore auf. „Wir konnten zeigen, dass Streptomyces acht bis zehn verschiedene Baupläne umsetzen kann, die sich chemisch geringfügig voneinander unterscheiden“, berichtet Julia Bandow. „Nun wollen wir herausfinden, wie die Produktion der unterschiedlichen Varianten dem Bakterium hilft, sich an verschiedene Umweltbedingungen anzupassen“, erzählt sie.
Bakterium unter Verdacht
All diese Erkenntnisse zusammengenommen, verdächtigen die Forschenden Streptomyces, Bacillus subtilis systematisch auszurauben. Es kann mit Ionophoren Eisen aus Bacillus subtilis schleusen und dieses mittels der Siderophore aufnehmen und so in sein Wachstum investieren.
Das wäre zwar ganz schön unsympathisch von Streptomyces. Sollte sich der Verdacht aber bestätigen, könnte sich diese Erkenntnis als nützlich erweisen. Denn Ionophore wie Calcimycin haben starke antibiotische Wirkung.
Wissenschaftsmagazin Rubin kostenlos abonnieren