Biologie
Enzymzwilling mit biotechnologischem Potenzial
Grünalgen besitzen zwei nahezu identische Wasserstoff produzierende Enzyme. Eines wird seit Jahrzehnten erforscht, das andere wurde kaum beachtet – bis vor Kurzem.
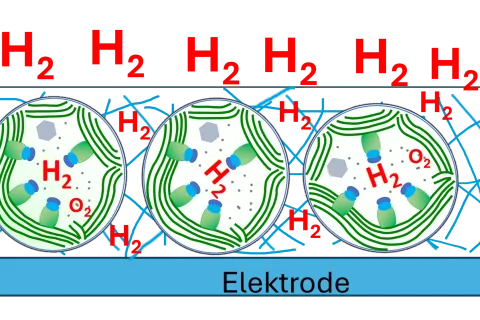
Wasserstoff produzierende Enzyme, sogenannte Hydrogenasen, könnten eine Quelle für regenerative Energie sein. Eine bislang kaum erforschte Hydrogenase der Grünalge Chlamydomonas reinhardtii hat die RUB-Arbeitsgruppe Photobiotechnologie nun genauer charakterisiert. Grünalgen besitzen zwei nahezu identisch aufgebaute Hydrogenasen. Obwohl sie sich in nur einer einzigen Aminosäure unterscheiden, haben sie doch unterschiedliche Eigenschaften, stellte das Bochumer Team fest. Die Ergebnisse beschreiben die Forschenden um Dr. Vera Engelbrecht und Prof. Dr. Thomas Happe in der Zeitschrift „International Journal of Hydrogen Energy“ vom 16. Dezember 2020.
Die Grünalgen-Hydrogenase CrHydA1 wird bereits seit Jahrzehnten erforscht. „Dass es im selben Organismus eine weitere Hydrogenase, CrHydA2, von nahezu identischer Bauweise gab, wurde lange als Kuriosum abgetan“, erzählt RUB-Forscherin Dr. Vera Engelbrecht. „Weil CrHydA2 deutlich niedrigere Wasserstoffproduktionsraten im Vergleich zu CrHydA1 aufwies und metabolisch scheinbar keine zusätzlichen Funktionen erfüllte, wurde dieses Enzym lange Zeit nicht näher charakterisiert. Nun haben wir bemerkenswerte Unterschiede feststellen können.“
Enzyme funktionieren in zwei Richtungen
Beide Enzyme können nicht nur Protonen und Elektronen zu Wasserstoff umsetzen, sondern auch die Rückreaktion katalysieren, also Elektronen aus der Oxidation von Wasserstoff gewinnen. Allerdings bevorzugen beide Proteine entweder die eine oder die andere Reaktion und weisen somit höhere Umsatzraten für jeweils eine Reaktionsrichtung auf. Während CrHydA1 eine stärkere Tendenz zur Wasserstoffproduktion zeigt, ergeben sich für CrHydA2 höhere Raten bei der Oxidation von Wasserstoff. Verantwortlich für diese Unterschiede ist eine einzige Aminosäure in der Nähe des aktiven Zentrums, die wie eine Art molekularer Schalter funktioniert.
„Eine solche Entdeckung kann von Nutzen für die biotechnologische Anwendung sein, weil Algen als lebende Fabriken zur lichtgetriebenen Produktion von chemischen Substanzen immer attraktiver werden“, erklärt Vera Engelbrecht. Energie, die zunächst in Form von Wasserstoff gespeichert wird, könnte mithilfe von Enzymen wie CrHydA2 wieder freigesetzt und für enzymatische Biokaskaden genutzt werden – etwa zur gezielten Produktion von Kosmetika, Medikamenten oder Lebensmitteln.