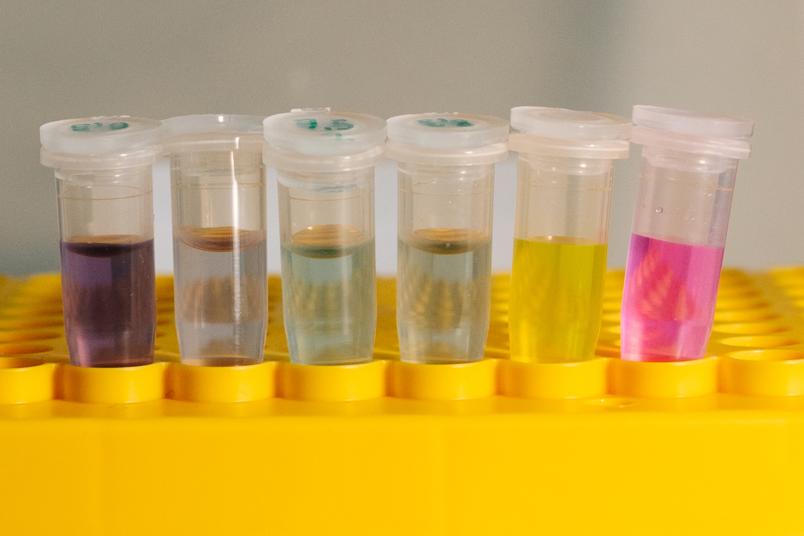
Kohlenstoff-Nanoröhren sind bunt. Ihre Farbpracht offenbaren sie aber nur, wenn eine wässrige Lösung ausschließlich Röhrchen mit einem bestimmten Durchmesser enthält.
Biochemie
Die Regenbogenfarben des Kohlenstoffs
Im Labor von Sebastian Kruss überrascht Kohlenstoff mit verschiedenen Farben. Die Bochumer Forschenden experimentieren mit den bunten Winzlingen für biomedizinische Anwendungen.
Wer an das Element Kohlenstoff denkt, hat in der Regel dunkle Farben vor Augen. Kohle – schwarz, klar. Oder das Graphit aus Bleistiftminen – grau. Wer funkelnde Edelsteine mag, denkt vielleicht auch an kristallklare Diamanten. Aber nur den wenigsten dürften bei dem Gedanken an Kohlenstoff die Farben des Regebogens durch den Kopf schießen. Doch auch so gibt es ihn, wie man im Labor von Prof. Dr. Sebastian Kruss feststellen kann.
Der Bochumer Physikochemiker experimentiert mit Kohlenstoff-Nanoröhren. Diese winzigen Röhren bestehen aus einem wabenförmigen Kohlenstoff-Geflecht und sind so klein, dass man sie mit bloßem Auge nicht sehen kann: 100.000-mal dünner als ein menschliches Haar. Eine wässrige Lösung aus beliebigen Kohlenstoff-Nanoröhren erscheint erwartungsgemäß schwarz. Aber trennt man die Röhrchen fein säuberlich nach unterschiedlichen Durchmessern auf, offenbaren sie ihre Farbpracht. Ein Durchmesser erzeugt eine gelbe Flüssigkeit, ein anderer eine grüne, der nächste eine blaue – und so weiter.
Nanoröhren als Sensoren
Nanoröhren-Lösungen sind aber nicht bloß hübsch anzuschauen, sie erfüllen in der Arbeitsgruppe Biophotonik und funktionale Materialien der Ruhr-Universität Bochum einen besonderen Zweck: Sie werden als Sensoren verwendet. Denn die Kohlenstoff-Winzlinge haben eine praktische Eigenschaft: Scheint sichtbares Licht auf sie, fluoreszieren sie. Das heißt, sie senden Licht einer anderen Wellenlänge aus, als eingestrahlt wurde, und zwar im Nahinfrarot-Bereich. Das Nahinfrarot liegt zwischen den für Menschen sichtbaren Wellenlängen und dem Infrarot-Bereich, den wir als Wärmestrahlung wahrnehmen.
Nahinfrarot-Aufnahmen
Nahinfrarot-Aufnahmen
„Dieser Wellenlängenbereich ist für viele Anwendungen interessant, zum Beispiel für die biomedizinische Diagnostik“, so Sebastian Kruss. Im Gegensatz zu sichtbarem Licht streut Nahinfrarot-Licht weniger. „Das heißt, wir können damit schärfere Bilder aufnehmen“, sagt er. „Außerdem kann das langwelligere Nahinfrarot-Licht tiefer in Gewebe eindringen als sichtbares Licht und ist dabei unschädlich.“
Anwendungen in der Biomedizin
Anwendungen sind viele denkbar: „Man kann mit den Kohlenstoff-Nanoröhren Strukturen im Körper sichtbar machen oder verschiedene Substanzen nachweisen“, gibt Kruss Beispiele. Mit seiner Gruppe hat er etwa gezeigt, dass sich der Botenstoff Dopamin, der eine wichtige Rolle bei der Parkinson-Erkrankung spielt, auf diese Weise detektieren lässt.

Sebastian Kruss leitet an der Ruhr-Universität Bochum die Arbeitsgruppe für Biophotonik und funktionale Materialien.
Um die Nanoröhren als Sensoren für körpereigene Stoffe zu nutzen, müssen die Forschenden sie zunächst biokompatibel machen. Dazu verpassen sie ihnen ein Kostüm. Sie beladen die Oberfläche mit Biopolymeren oder wickeln ein DNA-Fragment herum, sodass die Nanoröhren aussehen, als würden sie zum Körper gehören. Diese Modifikation dient aber noch einem weiteren Zweck: Indem die Forschenden die Röhrchen in eine Verpackung hüllen, können sie auch Bindestellen für beliebige Substanzen einbauen – etwa für Dopamin.
Bindung verändert Leuchten
Trifft ein Dopamin-Molekül auf eine passend modifizierte Nanoröhre, dockt das Dopamin an der Oberfläche des Röhrchens an, was deren Leuchten im Nahinfrarot-Bereich verändert; es leuchtet heller. Diesen Unterschied können die Biochemikerinnen und Biochemiker mit eigens dafür gebauten Mikroskopen erfassen.
Wie Wassermoleküle das Leuchten verändern
Wie Wassermoleküle das Leuchten verändern
So gelang es den Forschenden, die Konzentration von Dopamin mithilfe der Kohlenstoff-Nanoröhren als Sensor zu messen. Und das nicht nur in einer standardisierten Pufferlösung, sondern auch die direkte Freisetzung aus Zellen unter Bedingungen wie im menschlichen Körper. „Letzteres ist viel komplizierter, weil zum Beispiel Blut alle möglichen Bestandteile enthält, die die Messung stören können“, verdeutlicht Kruss.
Präzise Messungen für die personalisierte Medizin
Anwendungen der Methode sind zum Beispiel für die personalisierte Medizin denkbar. Menschen mit Parkinson-Krankheit erhalten zur Behandlung häufig L-Dopa, eine Vorstufe des Dopamins. „Die L-Dopa-Menge muss sich in einem bestimmten therapeutischen Fenster bewegen“, erläutert Sebastian Kruss. Eine zu geringe oder zu hohe Menge wirkt sich negativ auf die Symptome aus. „Eine bestimmte Dosis kann für einen Patienten optimal sein, für eine andere Patientin aber nicht“, führt der Biochemiker weiter aus. „Es gibt unter anderem Geschlechtsunterschiede.“
Dieses Problem ließe sich lösen, wenn man die L-Dopa-Konzentration einfach messen könnte – zum Beispiel über Kohlenstoff-Nanoröhren. „Ein solcher Test könnte ähnlich wie ein Glukosetest ablaufen, indem man einen Tropfen Blut abnimmt und die Messung außerhalb des Körpers macht“, so Kruss. Die L-Dopa-Menge könnte je nach Bedarf variiert werden, so wie Menschen mit Diabetes die Insulin-Menge nach einem Blutzucker-Test anpassen können. Die Forschenden zeigten bereits, dass L-Dopa in menschlichem Serum messbar ist. Außerdem konstruierte das Bochumer Team in Zusammenarbeit mit dem Fraunhofer Institut für mikroelektronische Schaltungen und Systeme in Duisburg ein kleines Auslesegerät für die Nanoröhren-Sensoren, das theoretisch mit einer Handykamera auslesbar ist. In Zukunft wollen die Wissenschaftlerinnen und Wissenschaftler die Technologie in Richtung eines Produktes weiterentwickeln.
Wissenschaftsmagazin Rubin kostenlos abonnieren
Wissenschaftsmagazin Rubin kostenlos abonnieren
Potenzielle Anwendungen der Nanoröhren-Sensortechnik beschränken sich aber nicht auf Dopamin-Messungen. Auch andere Stoffe können damit nachgewiesen werden, etwa solche, die die Anwesenheit bestimmter Bakterien oder Viren verraten. Zudem kann die Bochumer Gruppe mit der Technik sichtbar machen, wie Nervenzellen miteinander kommunizieren.
Mit Pflanzen kommunizieren durch Nanoröhren
Das Team erprobt aber auch an einen Einsatz jenseits der Biomedizin und testet die Kohlenstoff-Nanoröhren als Pflanzen-Sensoren. „Unsere Vision sind smarte Pflanzen“, sagt Kruss. „Wir können sie mit Nanosensoren ausstatten und mit ihnen kommunizieren, um herauszufinden, was ihnen fehlt.“
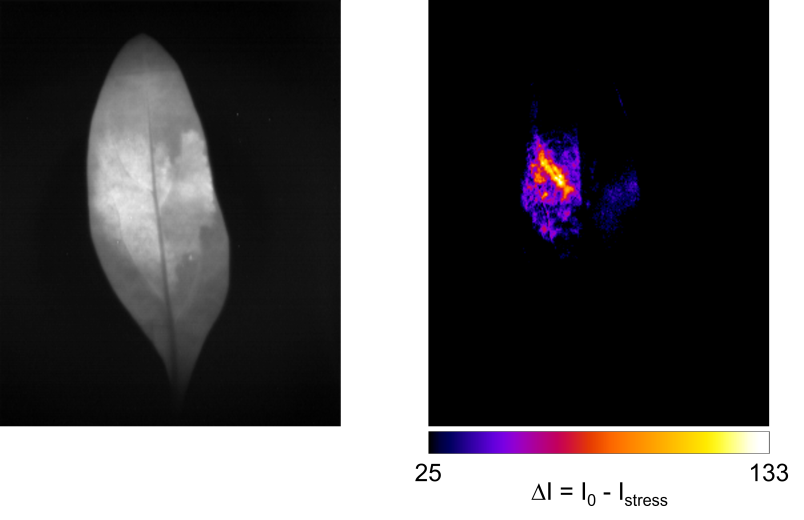
Links ist eine Nahinfrarot-Aufnahme eines Pflanzenblatts mit Sensoren zu sehen. Rechts ist farbcodiert angezeigt, an welchen Stellen des Blatts die Pflanze reaktive Sauerstoffspezies als Zeichen für Stress ausschüttet. Je heller die Farbe, desto höher der Stress.
Durch Hitze oder Trockenheit gestresste Pflanzen schütten reaktive Sauerstoffspezies aus, deren Anwesenheit das Leuchten der Nanoröhren verändert. Gegen Schädlinge verteidigen sich Pflanzen, indem sie bestimmte Substanzen absondern – die sich genau wie die Sauerstoffspezies mit Nanoröhren nachweisen lassen. „Die Idee ist, sehr genau feststellen zu können, was einer Pflanze fehlt, um dann präzise und ressourcensparend die richtigen Maßnahmen einleiten zu können“, skizziert Sebastian Kruss das Fernziel dieser Forschung. Das sind doch alles andere als kohleschwarze Aussichten.











