
Die transparenten Zylinder und die kleinen Teflonkugeln entwickelten die Forschenden für die Experimente selbst.
Fotochemie
Geschüttelt statt gerührt
Der richtige Move ermöglicht lichtgetriebene Reaktionen ohne umweltschädliche Lösungsmittel.
Um chemische Reaktionen in Gang zu bringen, braucht es Energie. Licht als Quelle zu nutzen, ist nachhaltig: Es ist unbegrenzt vorhanden und nicht umweltschädlich. „Der Nachteil ist, dass fotochemische Reaktionen in der Regel in Lösung stattfinden, und zwar in starker Verdünnung“, sagt Carolina Spula. Lösungsmittel sind ein bedeutendes Umweltproblem. Spula verzichtet deswegen darauf. Am Lehrstuhl Anorganische Chemie I bei Prof. Dr. Lars Borchardt arbeitet sie an der Feststoff-Fotochemie. Reaktionen laufen dabei sozusagen trocken ab: lösungsmittelfrei und lichtbetrieben. Es sind jedoch einige Hürden zu überwinden.
„Bisher war man bei der Feststoff-Fotochemie auf sehr kleine Mengen begrenzt“, erläutert Carolina Spula. Da das Licht nicht tief in einen Feststoff – häufig ein Pulver – eindringt, konnte man zum Beispiel nur ganz dünne Pulverschichten auf ein Glasplättchen auftragen und das dann von unten beleuchten. Wie aber kann man dafür sorgen, dass auch größere Mengen Pulver überall ausreichend Licht abbekommen, um reagieren zu können?

Carolina Spula fertigt ihre Doktorabeit in der Arbeitsgruppe Mechanochemie an.
Carolina Spula setzt auf Bewegung. Sie entwickelte in ihrer Doktorarbeit spezielle Fotoreaktoren für Kugelmühlen, um die aus einem transparenten Quarzglaszylinder und mehreren kleinen Teflonkugeln bestehenden Reaktionsgefäße während des Schüttelns bestrahlen zu können. Den Ausgangsstoff für die gewünschte lichtgetriebene Reaktion füllt sie in Pulverform hinein. Der Zylinder wird mit Kunststoffdeckeln verschlossen. Dann wird das Röhrchen quer in einen Apparat eingespannt, der es horizontal schüttelt, während es von allen Seiten von mehreren UV-Lampen beleuchtet wird.
Ein Drittel Pulver, ein Drittel Kugeln, ein Drittel Luft
Mit diesem Aufbau experimentierte Carolina Spula im Rahmen ihrer Doktorarbeit und perfektionierte ihn. „Als Faustregel kann man sagen: Für eine erfolgreiche Reaktion braucht man ein Drittel Bechervolumen Pulver, ein Drittel Kugeln und ein Drittel Luft“, berichtet sie. „Bei manchen Reaktionen kann es auch hilfreich sein, ein wenig Füllstoff hinzuzufügen, etwa ein inertes Salz. Das verhindert, dass sich Pulver in einer Ecke zusammenklumpt, wo es kein Licht mehr abbekommt.“ Der Füllstoff lässt sich später einfach wieder abtrennen. Gelegentlich nutzt die Forscherin auch eine kleine Menge Lösungsmittel, sodass im Röhrchen eine Art Paste entsteht.
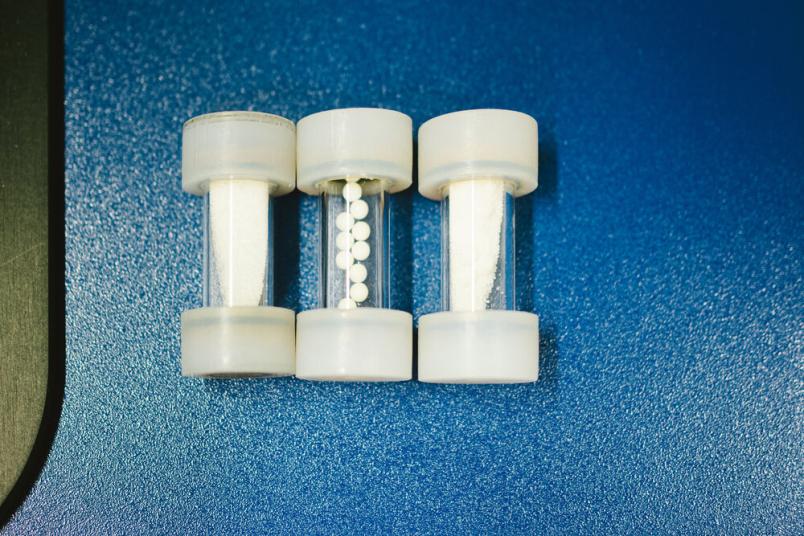
Die Faustregel lautet: Ein Drittel Pulver, ein Drittel Kugeln, ein Drittel Luft. Verzichtet man auf die Kugeln, kann man mehr Pulver einfüllen.
Um größere Pulvermengen behandeln zu können, probierte Carolina Spula eine andere Methode aus, den Röhrcheninhalt in Bewegung zu versetzen: den resonant akustischen Mixer. Hier wird das Röhrchen aufrecht eingespannt und vertikal in Schwingungen versetzt. „Das ist in etwa so wie bei den Farbmischanlagen, die es in Baumärkten gibt“, veranschaulicht sie. Der Inhalt des Röhrchens wird dabei so durchmischt, dass sich ein Hauptstrom bildet, daneben aber noch mehrere kleinere Turbulenzen entstehen. Dadurch mischt sich alles gut durch und jeder Pulverpartikel gelangt irgendwann so weit nach außen an die transparente Wand des Röhrchens, dass das Licht ihn erreichen kann. Da man dabei keine Kugeln benötigt, kann man mehr Pulver ins Röhrchen füllen.
Die Reaktionen, auf die es Carolina Spula abgesehen hat, sind alle organischer Natur. Ein Beispiel ist die Cyclodehydrochlorierung. Dabei wird von einem chlorierten Vorläufer-Kettensystem aus Kohlenstoffringen ein Chloratom abgespalten, sodass sich genau an dessen Position die dritte Kohlenstoffkette zu einem Ring schließt. Die Bindung des Chlors an den Kohlenstoff ist deutlich schwächer als die Bindung zwischen den Kohlenstoffatomen. Die Lichtteilchen versetzen die für die Bindung verantwortlichen Elektronen in einen angeregten Zustand, sodass die Bindung aufbricht – und zwar nur diese Bindung und keine andere. Automatisch schließt sich dann der Kohlenstoffring an genau der richtigen Stelle.
Nanographene könnten Silizium ablösen
„Hintergrund ist, dass man möglichst lange, planare Kohlenstoffketten haben möchte“, erklärt Carolina Spula. Solche sogenannten Graphen-Nanoribbons könnten aufgrund ihrer einstellbaren Bandlücke das Potenzial haben, eines Tages Silizium-Halbleiter in der Mikroelektronik zu ersetzen. Die Bandlücke des Siliziums ist begrenzt. Kohlenstoff könnte diese Grenze heraufsetzen.“
Bei den Nanographenen kommt es auf eine präzise Geometrie an: Sie müssen absolut plan sein. Damit sich die Kohlenstoffringe bei der Herstellung aus einem Vorgängermolekül nicht durch Verdrehung des Moleküls auf dessen Rückseite schließen, wird mit dem Chlor oder einem ähnlichen Element eine Art Sollbruchstelle eingebaut.

Von allen Seiten mit speziellem UV-Licht bestrahlt werden die Reagenzien gemeinsam mit kleinen Kugeln in den Mahlbechern horizontal geschüttelt.
Solche Reaktionen sind zwar auch auf andere Weise in Lösung möglich. Doch je größer die Kohlenstoffring-Kette, desto schlechter löst sie sich. „Um dieses Problem zu umgehen, muss man dann immer harschere, noch schlechter umweltverträgliche Lösungsmittel benutzen“, erklärt Carolina Spula.
Bei der fotochemischen Herstellung des Nanographens ist das kein Problem. „Für die Umwandlung von 150 Milligramm eines Dreierrings haben wir in der Mühle 25 Stunden gebraucht“, berichtet sie. „Die Reaktion eines doppeltchlorierten Fünfringsystems war nach 48 Stunden abgeschlossen.“ Dass die gewünschte Reaktion im Pulver passiert war, wies die Chemikerin mittels geeigneter Analysemethoden wie Kernspinresonanz-Spektroskopie nach.
„Bislang haben wir das alles nur im Labormaßstab durchgeführt“, so Carolina Spula. „So konnten wir zeigen, dass das Verfahren funktioniert.“ Interessant könnte es auch für andere Anwendungen der organischen Synthese sein, zum Beispiel bei der Herstellung von Düngemitteln oder pharmazeutisch wirksamen Verbindungen ganz ohne die Verwendung metall-basierter Katalysatoren.
Übertragung auf industriell interessante Bindungen
In ihrer Dissertation widmete sie sich der Frage, ob sich die Methode nur auf Ringschlussreaktionen beschränkt oder auch für die generelle Funktionalisierung von Bindungen zwischen Kohlenstoff und Halogenen wie Chlor, Brom oder Iod, sogenannte C-X Bindungen, nutzen lässt. „Klassische C–X-Funktionalisierungen benötigen meist Übergangsmetalle und gefährliche Reagenzien, was Kosten, Abfälle und Umweltbelastungen verursacht“, sagt Carolina Spula. „Fotochemische Alternativen sind zwar bekannt, benötigen aber stark verdünnte Lösungen.“
Sie entwickelte eine metall- und katalysatorfreie Synthesevorschrift für die fotochemische Bindungsbildung zwischen Kohlenstoff und Bor zur Herstellung von Arylboronsäureestern, einer wichtigen Molekülklasse in der organischen Synthese, der Sensorik, bei der Herstellung von Arzneistoffen und in den Materialwissenschaften. Das Protokoll konnte sie auf Kohlenstoff-Phosphor- und Kohlenstoff-Schwefel-Bindungen erweitern. Diese Molekülklassen finden unter anderem Anwendung in der Pharmazie und der Agrarwirtschaft als Dünger. „Die Auswertung hat gezeigt, dass unsere UV-unterstützte mechanochemische Methode im Vergleich zu lösungsmittelbasierten oder metallkatalysierten Methoden die besten Ökobilanzwerte bei geringstem Energieverbrauch aufweist“, berichtet die Forscherin.
Wissenschaftsmagazin Rubin kostenlos abonnieren






